Polski start-up Selvita poinformował o tym, że amerykańska Agencja ds. Żywności i Leków (FDA) zdecydowała o zawieszeniu badań klinicznych nad jednym z elementów jego leku. Dla krakowskiej spółki to spory problem, ponieważ sytuacja ta zagraża kwestii wypuszczenia medykamentu na rynek. W efekcie notowania Selvity na warszawskiej giełdzie runęły o kilkanaście procent.
REKLAMA
Na wprowadzenie do sprzedaży wynalazku Selvity czekają chorzy na białaczkę z całego świata. Specjalistom polskiego start-upu udało się stworzyć cząsteczkę SEL24, która ma się stać ważnym elementem medykamentu do leczenia ostrej białaczki szpikowej. W projekt uwierzyła włoska firma Menarini, która jest jednym z kilkudziesięciu największych przedsiębiorstw farmaceutycznych na świecie. Włosi wyłożyli już 20 mln złotych, a w przypadku pomyślnego przebiegu badań mają dołożyć kolejne 380 mln zł. Problem w tym, że te utknęły właśnie w martwym punkcie.
Kłody pod nogi rzucają Amerykanie. – Decyzja FDA została wydana po wystąpieniu zgonu pacjenta w następstwie udaru, który wcześniej przyjmował SEL24, które zostało zaraportowane jako SUSAR (ang. Suspected Serious Unexpected Adverse Reaction – podejrzewane niespodziewane poważne działanie niepożądane). Związek tego zdarzenia z SEL24 został oceniony przez lekarza prowadzącego jako możliwy – poinformowała Selvita. Przedstawiciele start-upu dodają jednak, że stan zmarłego pacjenta był bardzo ciężki, a on sam brał wcześniej udział w testach dwóch innych leków.
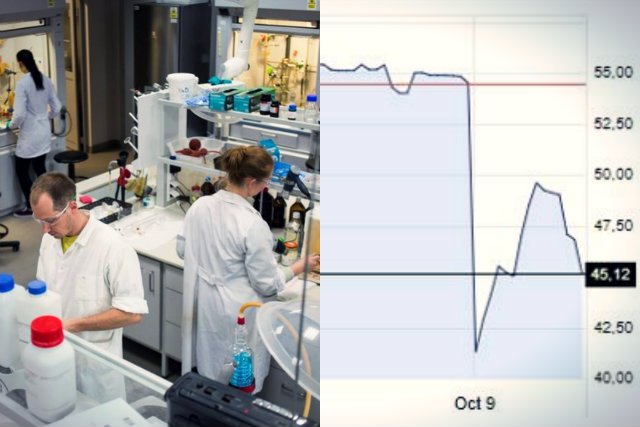
FDA oczekuje teraz od krakowskiej spółki przedstawienia dodatkowych danych i wprowadzenia poprawek do protokołu badania. Inwestorom te niepokojące wieści nie przypadły jednak do gustu. Tuż po ogłoszeniu niepomyślnej decyzji amerykańskiej agencji, akcje Selvity na warszawskiej Giełdzie Papierów Wartościowych spadły o ponad 17 proc. Krakowianie uspokajają jednak, że istnieją spore szanse na rychłe wznowienie badań – ich zdaniem powinno to nastąpić w ciągu najbliższych 2-3 miesięcy.
